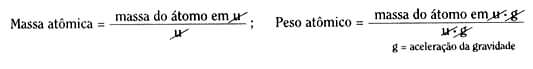|
Comentários e Observaçőes
sobre o Cap. 15 de A Grande Síntese
A EVOLUÇĂO DA
MATÉRIA POR INDIVIDUALIDADES QUÍMICAS - O HIDROGĘNIO E AS NEBULOSAS |
Neste capítulo Ubaldi inicia a descriçăo da evoluçăo da matéria no nosso Universo. Descreve as
diversas formas que g assume, caracterizando
a individualidade de cada elemento químico, distinguindo-o por suas qualidades. Mas ao mesmo
tempo mostra as relaçőes e parentescos entre os 92 elementos da Tabela Periódica. Quando
escreveu este texto a cięncia ainda năo conhecia todos os 92 elementos, mas, mesmo assim,
Ubaldi mostra os seus lugares na Tabela e indica seus números atômicos. Hoje, todos estes
elementos săo conhecidos e suas características se harmonizam com as
relaçőes e princípios revelados por Ubaldi.
Dissemos anteriormente que, devido ao avanço
científico, o homem conseguiu criar mais 18 elementos artificiais, totalizando hoje 110
elementos químicos conhecidos. No capítulo 18 Ubaldi previu a continuidade da série de
elementos químicos além do U e aquém do H.
O Hidrogęnio H, cujo peso atômico é 1,008, é o ponto de
partida da série dos elementos químicos.
Mas, aqui é preciso esclarecer um ponto que para
muitos significa um equívoco nos conceitos estabelecidos neste capítulo. Estamos referindo ao
emprego, por Ubaldi, da noçăo de Peso atômico em vez de Massa atômica. Pergunta-se: será que Ubaldi confundiu duas coisas diferentes já que massa se refere a quantidade de
matéria e peso é a força de atraçăo que a Terra exerce no corpo? O peso de um corpo na Lua
seria 6 vezes menor que na Terra, mas a massa seria a mesma. Alguém poderia afirmar que A
Grande Síntese foi escrita no início da década de 30 e nesta época muitos compęndios de Química
ainda confundiam massa com peso daí o erro de interpretaçăo de Ubaldi. Ledo engano! Ubaldi
nunca poderia estar errado, pois A Grande Síntese é um livro inspirado pelo Alto e por isso
mesmo isento de erros. Ao contrário, Ubaldi estava muito além do seu tempo como está
demonstrado abaixo: Modernamente massa atômica é por definiçăo o número que indica quantas
vezes a massa do átomo é maior que a unidade de massa atômica (u). Assim para encontrarmos a
massa atômica temos de dividir a massa do átomo por u, entăo a massa atômica é um número puro
(adimensional) de valor idęntico ao peso atômico.
A definiçăo de valęncia está de acordo com a Química da época
em que foi escrita A Grande Síntese.
Neste tempo ainda năo se conhecia a distribuiçăo das camadas eletrônicas do átomo, por isso se
definia a valęncia em funçăo do Hidrogęnio H. Hoje se define da seguinte forma: A
valęncia de um elemento químico é o número de ligaçőes iônicas ou covalentes, que um átomo
desse elemento é capaz de estabelecer. Mas se comparáramos a definiçăo de A Grande
Síntese com a definiçăo moderna veremos que conceitualmente ambas estăo corretas. A
diferença está na maior precisăo da definiçăo moderna na explicaçăo porque dois ou mais
elementos apresentam valęncias diferentes quando formam dois ou mais compostos químicos. É o
caso, por exemplo, da valęncia do Ferro (Fe) nos compostos OFe e O3
Fe2.
Se se
considerarmos que A Grande Síntese é um livro inspirado alguém poderia questionar a
definiçăo menos precisa de Ubaldi sobre a valęncia dos elementos químicos. A explicaçăo é
simples: Ubaldi năo poderia expor conceitos que ainda năo eram conhecidos. Caso empregasse
definiçőes que escapassem ao conhecimento da cięncia da época, sua obra năo seria compreendida
pelos seus contemporâneos. Como tudo muda, os próprios conceitos que ora adotamos, evoluirăo no
futuro para formas cada vez mais precisas, assim de nada adiantaria avançar muito, pois o
conhecimento sempre será relativo. Outro ponto a considerar é que a revelaçăo que nos vem
através de A Grande Síntese tem o objetivo de reorientar a marcha evolutiva e năo a de
nos eximir do esforço da conquista do conhecimento.
Ubaldi emprega a definiçăo de peso atômico adotada na
época, ou seja, sendo o átomo uma entidade muito pequena, o seu peso atômico năo pode ser
medido diretamente, estabelece-se entăo uma relaçăo entre o peso de cada elemento químico e o
peso do átomo de hidrogęnio tomado como padrăo, atribuindo, por convençăo, o valor igual a 1
para este peso. Com o descobrimento dos isótopos foi necessário a mudança do padrăo. Desta
forma foi definido o novo padrăo, conhecido como unidade padrăo de massa (u). Essa
mudança de padrăo foi necessária porque foi descoberto que o Hidrogęnio é constituído por tręs
isótopos de massas diferentes, fato que ocasionava uma pequena imprecisăo nos cálculos.
Muita gente estranha a afirmaçăo de
Ubaldi sobre o inflexível negativismo do Hidrogęnio alegando que o hidrogęnio é um íon positivo e năo negativo. Năo seria, ao
contrário, o inflexível positivismo do Hidrogęnio? Esta objeçăo é outro engano ocasionado pelo
desconhecimento do que seja realmente negativismo químico, ou melhor, Eletronegatividade.
O livro Química Integral de
Martha Reis define eletronegatividade como a capacidade que um átomo possui de atrair
elétrons para perto de si, em comparaçăo a outro átomo. Existe uma escala de
Eletronegatividade, denominada escala de Linus Pauling em que a negatividade do
Hidrogęnio é representada por um número maior que 2 numa escala que vai de zero a 4.
Mais adiante no mesmo livro de Química
encontramos uma explanaçăo sobre as propriedades químicas do Hidrogęnio: "O Hidrogęnio é
um elemento atípico totalmente diferente dos outros. É o menor e o mais leve dos átomos. Possui
uma única camada eletrônica (camada K) contento apenas um elétron. Por causa disso, o
Hidrogęnio é normalmente colocado na tabela periódica junto ŕ família dos metais alcalinos
(elementos que possuem um elétron na camada de valęncia). O Hidrogęnio, entretanto, năo possui
nenhuma das propriedades que caracterizam esses metais; pelo contrário, sua tendęncia é atrair
mais um elétron para completar a sua primeira e única camada (uma vez que a camada K fica
completa com 2 elétrons). (.....) O ideal é matę-lo ŕ parte, destacado da tabela periódica"
(Como fez Ubaldi!!!).
Desta
forma o Hidrogęnio pode estabelecer ligaçőes iônicas com metais eletropositivos, pois os metais
perdem elétrons para adquirir estabilidade e podem formar compostos iônicos com o Hidrogęnio
(exemplo: MgH2). Por outro lado o Hidrogęnio possui também eletropositividade ou caráter
metálico que lhe permite a formaçăo de cátions (íons positivos) que em soluçőes eletrolíticas
migram para o pólo negativo (cátodo). Explica-se assim, o seu caráter atípico,
como foi dito acima e também sua "inflexível negatividade" na expressăo de
Ubaldi.
Para apoiar sua
afirmaçăo de que foi a partir do Hidrogęnio que se originou, por evoluçăo, os outros elementos
químicos, Ubaldi descreve o desenvolvimento das Nebulosas, onde se pode verificar pela análise
espectral a composiçăo química das várias etapas evolutivas atravessada pela matéria
constituinte da nebulosa. Verifica-se, entăo, que os corpos estelares mais jovens săo compostos
apenas pelo Hidrogęnio, posteriormente pelo envelhecimento e esfriamento paulatino destes
corpos văo surgindo na sua constituiçăo elementos químicos mais pesados. Demonstra também que a
matéria é um inversăo da energia ao constatar que os corpos irradiantes de energia luminosa a
medida que se esfriam tornam-se mais densos, deixam de emitir energia e săo formados por
elementos químicos mais pesados. Na evoluçăo das nebulosas pode-se, entăo, ser observado, além
do transformismo involutivo b®g a
evoluçăo dos elementos químicos (g) a partir
do Hidrogęnio (H) até os elementos mais pesados como o Urânio (U), ponto em que
se inicia o retorno de g a b pela desintegraçăo da matéria pela radioatividade.
Outro ponto importante do
transformismo evolutivo do Universo, a continuidade, é ressaltado aqui. Esta
continuidade năo acontece de maneira seqüencialmente homogęnea e sim em forma de individuaçőes
bem definidas: "essa continuidade tem paredes e vértices". É lógico que tudo tem que ser
individuado num Universo de estrutura hierarquizada. Se assim năo fosse o universo seria
semelhante a uma infinita planície deserta, onde năo existe nada, uma planície tăo igual que é
impossível estabelecer qualquer ponto de referęncia ou de distância, nesse espaço
incomensurável.
Em virtude desta
característica individualizante que perpassa todo o Universo, a matéria também năo poderia
fugir a esta regra, assim ela assume - tanto nos elementos simples como nos compostos - formas
rigorosamente individualizadas. Desta modo é perfeitamente coerente falar-se em indivíduos
químicos como se fala sobre as individualidades vegetais e animais. Sobre estes fundamentos
desenvolveu-se, entăo, a cięncia química estabelecendo a classificaçăo destas individuaçőes
químicas e as leis que regem suas interaçőes. As leis citadas, como a lei da espécie química
mostram com clareza a exata regularidade no comportamento dos elementos químicos, simples
e compostos.
Pedro
Orlando Ribeiro
http://www.monismo.com.br